Update: as regras para agrupamento de produtos em ortopedia estão em revisão, por meio da Consulta Pública nº 1042 de 08/04/2021. Implantes ortopédicos possuem regras de agrupamento especiais determinadas pela ANVISA, definidas pela RDC 59/2008 e pela IN 01/2009. Essas regras de agrupamento determinam quais produtos podem ficar agrupados em um único registro de família ou de sistema. Especificamente quanto a placas e parafusos ortopédicos, as regras são minuciosas podem confundir um pouco. Mas, cuidado! Erros de enquadramento podem ser vistos pela ANVISA como motivo para indeferimento sumário da petição de registro. Portanto, seguem abaixo três dicas para definir o enquadramento e a separação dos produtos em diferentes registros. Parafusos Canulados devem ser registrado em separado, com apenas duas exceções O principal uso de parafusos canulados em ortopedia é providenciar compressão óssea. Esse tipo de parafuso canulado é geralmente colocado no osso de maneira isolada (stand-alone), isto é, sem contato com placas ou outros dispositivos. Assim, devido às regras da IN 01/2009, eles não podem formar família com outros parafusos sólidos, e, portanto, devem ser registrados à parte. As duas únicas exceções são: a) parafusos pediculares para coluna, que podem (e devem) ser registrados em conjunto com o sistema (barras, ganchos…). b) parafusos canulados que possuem mecanismo de bloqueio, e servem para serem inseridos em furos de placas ósseas, formando um sistema bloqueado. Cuidado com a divisão entre “mini/micro fragmentos” e “grandes/pequenos fragmentos” para sistemas de placas e parafusos A IN 01/2009 determina que o diâmetro de Ø 2.7 é o tamanho de corte, sendo que sistemas de placas e parafusos de diâmetro igual ou menor que Ø 2.7 mm devem ser considerados mini/micro, enquanto sistemas maiores de Ø 2.7 mm devem ser considerados grandes/pequenos, e esses dois grupos devem ser registrados em separado. A “pegadinha” é que, se um fabricante possui um sistema de placas e parafusos, onde o parafuso tem Ø 2.7mm, a interpretação inicial é que se trata de um sistema de mini/micro fragmentos. Porém, a IN 01/2009 é clara ao estabelecer que o que vale é o diâmetro do furo na placa. Assim, se o parafuso possui Ø 2.7 mm, em geral o tamanho nominal do furo é um pouco maior do que isso (por exemplo, Ø 3.0 mm), o que faz o sistema se classificar como grandes/pequenos fragmentos. Placas / Parafusos de aço ou titânio podem ficar no mesmo registro Precisa separar o registro de placas e parafusos de aço do registro dos mesmos produtos em titânio? A resposta é: não precisam ser registros separados. A RDC 59/2008 é clara em determinar que produtos de matérias-primas diferentes precisam estar em registros separados, porém logo a seguir estabelece que a separação que deve ocorrer é entre produtos metálicos, poliméricos e cerâmicos. Assim, como aço e titânio são materiais metálicos, podem ficar no mesmo registro. Via de regra, esses produtos não são intercambiáveis (por exemplo, parafusos de aço não podem ser usados em placas de titânio, e vice-versa), porém isso não impede o registro em conjunto, já que essa questão pode ser abordada por uma tabela de compatibilidade entre os produtos objeto de registro. Por outro lado, manter registros em separado (um registro para o sistema de aço e outro para o sistema de titânio) também não é proibido, e muitas vezes é usado como estratégia comercial, já que muitos compradores usam o número de registro ANVISA como parâmetro para comparação de preços. Caso queira estabelecer uma estratégia de separação de registro para produtos em ortopedia, ou outros, faça contato conosco! *Esse post está sendo publicado em Abril de 2021, e as regras são dinâmicas e passíveis de alteração. Mantenha contato conosco para dicas atualizadas!
MSC MED tem projeto aprovado pela FINEP
A Financiadora de Estudos e Pesquisas é uma agência pública que financia a inovação, desde a pesquisa básica até a preparação do produto para o mercado. O projeto idealizado e elaborado pela MSC MED (Florianópolis, SC) em parceria com a fabricante de implantes cirúrgicos SARTORI (Rio Claro, SP) foi um dos 11 selecionados pela FINEP dentre centenas de propostas submetidas na temática Saúde 4.0 – Edital Tecnologias 4.0. O projeto, classificado em sexto lugar, terá recursos de subvenção aportados pela instituição e reforça a posição da MSC MED como Startup de referência em inovação de tecnologias médicas.
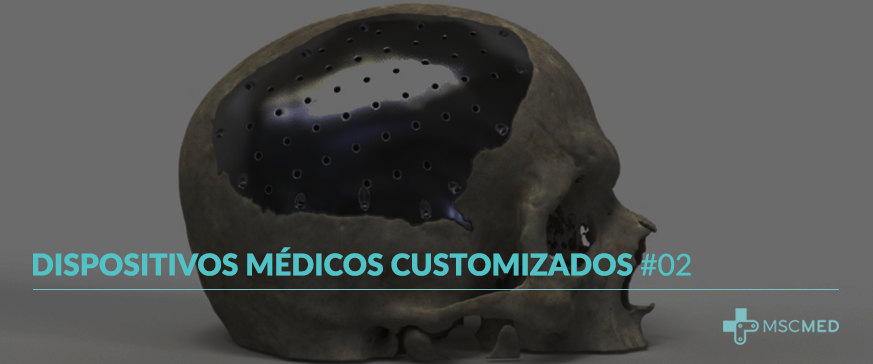
Dispositivos Médicos Customizados #02
Você já conferiu aqui a primeira parte do nosso conteúdo sobre produtos médicos customizados. A MSC MED é pioneira na definição de metodologias de avaliação de projetos customizados ao paciente, e podemos auxiliar na avaliação de segurança e eficácia do seu projeto. Porém, para navegar por esse tema, é importante entender como são classificados os dispositivos customizados. A ANVISA divide os dispositivos personalizados, aqueles feitos especificamente para um paciente, em: a) Dispositivos Médicos Sob Medida b) Dispositivos Médicos Paciente-Específico De acordo com a RDC 305/2019, há uma diferença muito relevante entre esses dois tipos de produto O Dispositivo Médico Paciente-Específico é aquele dispositivo médico personalizado feito “em escala”. Ele é caracterizado por estar definido dentro de um “domínio de projeto”. Isto é: existem regras específicas para projetá-lo, e ele, ainda que seja personalizado ao paciente, tem dimensões máximas e mínimas previstas e regras que possibilitam uma certa previsibilidade ao processo. Assim, o processo de customização pode ser feito em escala, sendo possível validá-lo. Esse tipo de produto pode ser registrado na ANVISA como um dispositivo médico paciente-específico, e ser comercializado, dentro de seus limites e regras de projeto, sem que seja necessário avisar a ANVISA a cada fabricação. Já o Dispositivo Médico Sob Medida é também um dispositivo médico personalizado, porém não é feito “em escala”. Ele é caracterizado por ser uma “exceção à regra”. É definido como um dispositivo feito sob prescrição médica, para um único caso, para um paciente que tem uma necessidade em especial. Assim, por atender a um caso único em específico, não é viável padronizar o processo de customização e de produção desse tipo de produto. Assim, esse dispositivo médico não é registrado a na ANVISA como um produto personalizado. Nestes casos, o fabricante precisa de uma prescrição médica para fabricar o produto (o médico é corresponsável pela segurança do produto), e é necessário que o fabricante possua um produto de mesma indicação de uso já registrado na ANVISA, o que demonstra que há expertise por parte deste fabricante para trabalhar com o assunto. Além disso, é necessário notificar a ANVISA a fabricação de um produto médico sob medida. No fim, tanto o dispositivo médico Sob Medida quanto o dispositivo médico Paciente-Específico são produtos projetados e fabricados considerando a anatomia e a particularidade de um paciente. Porém, sob um ponto de vista de controle de qualidade, controle de projeto, classificação sanitária e escala comercial, esses produtos são bastante diferentes. Portanto, fique sempre atento! A melhor estratégia regulatória varia a cada caso. Se precisar de ajuda, conte conosco!
Dispositivos Médicos Customizados #01
A Medicina Personalizada é uma realidade. Hoje, é possível desenhar dispositivos médicos, incluindo implantes, de acordo com a anatomia de cada paciente, com base em exames de imagem. Isso possibilita a criação de uma gama de soluções que antes não eram possíveis, como por exemplo: a) placas para cranioplastia que mantém a simetria craniana do paciente, causando um efeito estético superior; b) próteses de joelho que seguem a anatomia do côndilo do paciente, levando a uma manutenção da curvatura natural do côndilo e provendo uma melhor sensação biomecânica ao paciente; c) guias para procedimentos cirúrgicos, onde regiões de corte ou de incisão podem ser definidas e apontadas de acordo com a anatomia interna do paciente, gerando cirurgias mais assertivas e menos invasivas. A ANVISA tem uma das legislações mais modernas do mundo quando o assunto são dispositivos médicos customizados, como estes. A RDC 305/2019, publicada pela ANVISA em Setembro de 2019, estabelece as regras para registro de dispositivos médicos personalizados. De maneira geral, a resolução estabelece que a avaliação de um produto personalizado não é muito diferente da avaliação de um produto “de prateleira”. Apenas, algumas regras adicionais, principalmente quanto a rastreabilidade e quanto a avaliação de segurança e eficácia, se aplicam. É natural que a rastreabilidade seja uma preocupação. Os produtos de prateleira, por serem iguais uns aos outros, podem ser intercambiados livremente entre si durante a fabricação, embalagem, expedição e logística. Já os produtos personalizados tem destino fixo: um paciente em específico. Uma troca durante o processo produtivo ou durante a logística pode causar consequências graves. Já a atenção especial quanto à comprovação de segurança e eficácia também é relevante. As empresas estão acostumadas a testar e avaliar produtos com design pré-estabelecido. Para um produto personalizado, que a cada paciente pode assumir uma forma, como garantir que o resultado final será sempre seguro e eficaz? Como a ANVISA endereçou estes e outros temas na RDC 305/2019 e como se adequar a eles? Na PARTE 02 desta série daremos mais detalhes! A MSC MED tem experiência no registro de dispositivos médicos customizados / personalizados na ANVISA. Se precisar de orientação, conte conosco.
Compatibilidade de Implantes Cirúrgicos em Ambiente de Ressonância Magnética
Atualmente, organismos reguladores têm dado muita atenção aos aspectos de desempenho de implantes cirúrgicos não-ativos em ambiente de ressonância magnética (RM). Historicamente, houve muita restrição para implantes ativos (marcapassos, por exemplo) quanto a riscos eletromagnéticos devido a presença de componentes eletrônicos no produto. Mas, quando se trata de implantes não-ativos, a admissibilidade de submeter pacientes ao ambiente de ressonância magnética mantém-se em discussão. Implantes fabricados de aço inoxidável, com características ferromagnéticas, são notadamente incompatíveis com ambiente de RM. Já para implantes fabricados com metais não-ferromagnéticos podem ser necessárias análises quanto aos riscos com base em métodos de ensaio e avaliações que identificam parâmetros como deslocamento induzido, aquecimento induzido e formação de artefato em diagnósticos por imagem. Para alguns implantes cirúrgicos de alta classe de risco, como os clipes de aneurisma, a realização de ensaios físicos de compatibilidade em ambiente de RM é obrigatória. Para diversos outros, a realização deste tipo de ensaio não é habitual. Produtos não-ferromagnéticos apresentam risco em MRI? Ferromagnetismo é o mecanismo básico pelo qual certos materiais, como o ferro, formam campos magnéticos permanentes, ou são atraídos por campos magnéticos. O fato de um implante ser fabricado de material não-ferromagnético não significa, entretanto, que não apresentará risco quanto a sua exposição a campo eletromagnético. Existem outros mecanismos de resposta a campos eletromagnéticos, como o paramagnetismo. Além disso, metais não ferromagnéticos ainda podem interferir nos campos criados pelos equipamentos de MRI e distorcer imagens de modo que elas não possam ser interpretadas de maneira apropriada. A maioria dos implantes ortopédicos, materiais e dispositivos avaliados para questões de MRI são feitos de materiais não-ferromagnéticos e, portanto, são potencialmente seguros ou condicionalmente seguros, quando respeitados os cuidados necessários. De acordo com estudos consultados, os implantes de titânio geram significativamente menos artefatos e levarão a melhores imagens de qualidade diagnóstica. Entretanto, devido ao comprimento do implante ou à formação de uma alça condutiva, o aquecimento induzido, relacionado ao procedimento de RM, pode ser um problema para alguns implantes ortopédicos, especialmente dispositivos de fixação cervical e sistemas de fixação interna ou externa. Adicionalmente a energia criada pela ressonância magnética pode causar problemas com qualquer metal condutor dentro de um implante, que pode inadvertidamente se tornar um transceptor de rádio. Quando isso acontece, o metal pode absorver a energia e começar a superaquecer, potencialmente danificando o implante e qualquer tecido que o rodeia. Como o FDA trata o tema De acordo com o FDA (Food and Drug Agency – EUA), para avaliação de implantes em ambiente de ressonância magnética, o fabricante pode declarar o seu produto como seguro, condicionalmente seguro ou não-seguro em ambiente de ressonância magnética. Para subsidiar a declaração, podem ser necessários racionais científicos, simulações computacionais e, até mesmo, ensaios físicos para diferentes intensidades de campo eletromagnético. Independente disso, os riscos associados à uma possível submissão de pacientes com implantes ao ambiente de RM precisam estar previstos no Gerenciamento de Riscos, de acordo com a norma ISO 14971. Há ganho comercial em afirmar que um implante é compatível? A tendência mundial é que sejam exigidos estudos mais completos sobre a compatibilidade de implantes não ativos em ambiente de RM. Reuniões técnicas estabelecendo as normativas sobre o tema estão em alto nível de atividade, os organismos notificadores da União Europeia têm sido rigorosos e há intensa troca de experiências no IMDRF. Naturalmente, médicos e pacientes irão preferir as próteses e implantes que foram avaliadas e atestam que são compatíveis com ambiente de ressonância magnética, trazendo maior segurança na tomada de decisões. Sendo assim, a realização de ensaios pode ser vista não apenas sob a ótica regulatória, mas também sob a ótica de diferencial de mercado. Avalie seu produto A MSC MED conta com especialistas focados em soluções que envolvem simulações computacionais para definição de casos críticos e comportamento de implantes em ambiente de RM, bem como estabelecimento de racionais baseados em literatura científica visando definir a necessidade e otimizar os testes físicos em cabine para avaliação do seu dispositivo médico em ambiente de RM. Estamos a disposição para atendê-lo. Referências Kumar, Ritabh, et al. “Safety of orthopedic implants in magnetic resonance imaging: an experimental verification.” Journal of orthopaedic research 24.9 (2006): 1799-1802. Koch, K. M., et al. “Magnetic resonance imaging near metal implants.” Journal of Magnetic Resonance Imaging 32.4 (2010): 773-787. ORTHOPEDIC Implants, Materials, and Devices. Disponível em: <http://www.mrisafety.com/SafetyInfov.asp?s_keyword=implant&s_Anywords=&SafetyInfoID=189>. Acesso em: 17 ago. 2018. THE FACTS About MRIs and Metal Implants. Disponível em: <https://www.verywellhealth.com/mri-with-a-metal-implant-or-joint-replacement-2549531>. Acesso em: 17 ago. 2018.